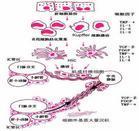
肝纤维化
肝纤维化(hepatic fibrosis)是指肝脏内弥漫性细胞外基质(特别是胶原)过度沉积。它不是一个独立的疾病,多种慢性肝脏疾病均可引起肝纤维化。
病因及发病机制
病因
肝纤维化(hepatic fibrosis)是指肝脏内弥漫性细胞外基质(特别是胶原)过度沉积。它不是一个独立的疾病,而是许多慢性肝脏疾病均可引起肝纤维化,其病因大致可分为感染性(慢性乙型、丙型和丁型病毒性肝炎,血汲虫病等),先天性代谢缺陷(肝豆状核变性、血色病、α1-抗胰蛋白酶缺乏症等)及化学代谢缺陷(慢性酒精性肝病、慢性药物性肝病)及自身免疫性肝炎、原发性肝汁性肝硬化和原发性硬化性胆管炎等。
发病机制
在正常肝组织中,各种细胞及细胞外基质万分有精确的相对比例和特定的相对空间位置,通过细胞之间、细胞与细胞外基质之间的信号传递精确地调控着结构、功能和代谢状态,成为一个相对稳定的微生态系统。从动态的观点来看,纤维增生是指各种细胞外基质合成增加,而纤维分解则是指细胞外基质的降解过程;肝纤维化的发生、发展和转归取决于二者的“净效应”。急性肝损害所致肝脏纤维增生是机体对于肝实质损伤的一种修复反应,一旦病因去除则过多的细胞外基质被降解,肝组织内细胞内细胞与基质万分恢复正常,因而不产生肝脏纤维化。但慢性肝病所致的持续或反复的肝实质炎症坏死可引起纤维结缔组织大量增生、而其降解活性相对或绝对不足,因此大量细胞外基质沉积下来形成肝纤维化。如果肝纤维化同时伴有肝小叶结构的破坏(肝再生结节),则称为肝硬化。但是,在临床上难以将两者截然分开,因为慢性肝病由肝纤维化到肝硬化是一个连续的发展过程。近年的基础和临床研究表明,如果能给予有效的病因治疗,或能直接抑制细胞外基质的合成和/或促进其降解,则已经形成的肝纤维化甚至早期肝硬化也是可以逆转的。
病理改变
表现为肝脏细胞外基质合成增多,降解减少。
临床特征
(2) 肝纤维化临床表现食欲减退,往往是最早症状,有时伴恶心,呕吐.
(3) 慢性消化不良症状,腹胀气,便秘或腹泻,肝区隐痛等,临床上部分患者无明显的慢性肝病史,肝纤维化临床表现原因不明出现上述消化不良症状,对症治疗效果不佳.经进一步检查才发现.
(4) 慢性胃炎,许多慢性肝炎患者出现反酸,嗳气,呃逆,上腹部隐痛及上腹饱胀等胃区症状.
(5) 肝纤维化临床表现出血,慢性肝炎由于肝功能减退影响凝血酶原及其他凝血因子的合成,肝纤维化临床表现常出现蜘蛛痣、鼻衄,牙龈出血,皮肤和粘膜有紫斑或出血点,女性常有月经过多.
伴发疾病
一般而言,慢性肝病因肝脏持续性损伤,多会伴有肝纤维化。我国慢性肝病中以慢性乙型肝炎最多,慢性丙型肝炎也不少见。这两类肝炎都因肝炎病毒复制,刺激了人体的免疫系统,造成免疫淋巴细胞在清除病毒时,“误伤”肝细胞,产生肝脏内炎症,诱导了纤维组织增生,致使肝纤维化。随着人民生活水平的提高,我国酒精性肝病和非酒精性肝病的发病率不断上升。这两种肝病中较重的病变是脂肪性肝炎,如不积极治疗,损伤的肝细胞也可刺激肝内纤维组织的大量增生,由肝纤维化发展到肝硬化。肝癌是各种肝病中最为凶险的疾病,常常同时伴有肝硬化。其他如药物性肝病、代谢性肝病、自身免疫性肝病或血吸虫病等,也与肝纤维化有染。由于每个患者体质情况和发病情况不一样,纤维化的程度与病情的程度或病程的长短可能不成正比关系。
肝纤维化的临床诊断
a、肝活检病理学检查:仍是诊断肝纤维化的金标准,是明确诊断、衡量炎症活动度、纤维化程度以及判定药物疗效的重要依据[1]。目前一般采用半定量计分系统。但是,由于肝纤维化在肝内分布不均匀,而且肝穿刺组织仅占全肝的五万分,可造成诊断误差。因此强调肝活检标本至少15 mm,并包含6个以上汇管区。Bedossa等[2]研究表明:按METAVIR计分系统标准,如肝穿组织为15 mm,肝纤维化诊断符合率为65%,如肝穿组织为25 mm,符合率为75%,因此主张不少于25 mm。另外肝活检是一种创伤性检查,穿刺后疼痛(24.6%)以及其他并发症使半数左右患者不愿接受该项检查。因此探索以非创伤性检查替代肝穿刺活检成为当务之急。
b、生化学检测:血清HA、 LN、 PCIII、CIV可反映肝纤维化程度,特别是HA和PCIII对早期肝纤维化的价值最高,同时也受肝脏炎症程度的影响。但有认为慢性丙肝患者HA水平与纤维化分级呈正相关,与肝脏炎症活动关系不大。也有认为CIV水平和肝纤维化及门脉高压程度关系较大,而与肝脏炎症活动关系较小。蔡卫民等[3]利用ROC曲线,对60例慢性乙肝患者肝活检病理组织学检查结果与血小板衍生生长因子BB(PDGFBB)、转化生长因子β1(TGFβ1)、基质金属蛋白酶抑制剂1(TIMP1)、基质金属蛋白酶1(MMP1)、 HA、 PCIII、CIV、LN和外周血单核细胞(PBMC)进行比较,结果表明:HA、 PCIII、 CIV、 LN有一定价值,血清PDGFBB的诊断价值最大。在筛选肝纤维化患者时,以血清PDGFBB和TIMPl mRNA联合检测最佳。另外国内外学者提出YKL40(人类软骨蛋白39)可用于评价肝纤维化程度[4]。 近年来推出的Fibrotest (FT)和ActiTest (AT)系统提供了评价肝纤维化的简便、非创伤性的检查方法,FT通过检测血中载脂蛋白A1、α2巨球蛋白、触珠蛋白和总胆红素,能简便、快速、准确定量评价肝纤维化的程度(FT值为0.00~1.00),而ActiTest (AT)系统,通过检测ALT和GGT,能定量评价肝脏的炎症坏死的程度(AT值也是0.00~100)[5-7]。Naveau等[6]对摄入酒精>50 g/d(平均100 g/d)的221例患者同时行肝穿刺活检、FT和HA检测。肝穿刺活检按METAVIR系统分级,其中明显肝纤维化(F2~F4)占63%。 FT的平均值:F0=0.29;F1=0.29;F2=0.40;F3=0.53;F4=0.88(除F0和F1之外,其余各组之间P值均<0.05)。而HA对F2和F1以及F2和F0之间无统计学上差异。 对F4的诊断,FT和HA的UROC (area under the ROC curves)都非常高,分别为0.95和093。Myers等[8]对209例HBV患者进行研究,其中61例(29%)纤维化分期为F2~F4,FT能正确作出评价(AUROC为0.78±0.04)。 FT积分在≤0.20和>0.80之间者,对肝纤维化的阳性和阴性预测值都是92%。因此认为只需要对FT>0.20和≤0.80之间的患者进行肝穿刺,以明确肝纤维化及其程度。Poynard复习了16篇文献后指出:对慢性HCV患者来说,FT和AT可以取代肝穿刺对肝纤维化和炎症坏死状况作出评价,肝穿刺应作为第二线,仅适用于对FT和AT结果有高度怀疑者[9]。
c、影像学检查:B超对肝脏表面、肝脏回声、肝静脉、肝边缘和脾脏面积5项参数与肝纤维化分期有很好的相关性,但对1~3期较难区分。也有人认为门静脉主干、门静脉每分钟血流量参数、脾厚度、脾静脉宽度及肝右叶最大斜径等参数的改变与肝纤维化的程度有较好的相关性。
彩色多普勒超声有助于评价肝纤维化的程度,因为肝纤维化时,肝动脉血流速度增加,门静脉血流速度减慢,因此二者(A/V)的比值能更全面地反映肝纤维化的血流动力学变化,优于单纯测定门静脉流速或肝静脉频谱改变的检测。Fibroscan(FS)是近年来推出的单维瞬变弹性图,是以超声(5 MHz )和低频弹性波(50 Hz )结合的测量组织硬度的仪器。由于肝脏的硬度与肝纤维化相关,因此反射波kPa越高,肝纤维化程度越重。Sandrin等[10]报道:FS的反射波≤5.1 kPa者,93%患者纤维化程度属于F0或F1,如反射波≥7.6 kPa,94%患者纤维化程度≥F2。Zio1等[11]报道:5例反射波≤3 kPa者,都是F1,而将反射波8.74 kPa、 9.56 kPa和14.52 kPa作为F≥2, F≥3和F=4的阈值,对肝纤维化有较高的敏感性和特异性。因此对反射波≥8.74kPa的患者需要治疗,无需进行肝穿刺。FS的局限性是不适用于腹水患者、肋间隙狭窄以及肥胖者。Castera等.[7].对183例慢性丙肝患者,同时检测FS、FT和ARPI,并和肝穿刺活检作对照。
按METAVIR分级F1=47; F2=53; F3=37; F4=46。FS值:F≥2 =7.1 kPa; F≥3=95 kPa;
F=4=12.5 kPa。结果显示:FS是检测肝纤维化的简单而有效的方法;同时检测FS和FT并与肝穿刺结果作比较,F≥2符合率为84%, F≥3为95%, F=4为94%。因此对大多数肝纤维化患者来说可避免肝穿刺。总之FS的优点是无创伤,患者无痛苦、无并发症,操作简便、快速(<5 min ),可在门诊或床边进行,由于量化,结果客观而可靠、重复性好。有望取代肝穿刺以诊断和监测肝纤维化的进程。
治疗
抗肝纤维化的药物治疗主要包括:
(1)针对原发病去除致病因素,如抗乙型肝炎、丙型肝炎病毒治疗、抗血吸虫治疗、戒酒等。
(2)针对肝纤维化本身的治疗,如通过抑制炎症或脂质过氧化,或者抑制肝星状细胞的增生活化,以及促进胶原降解等。目前已发现了具有抗纤维化作用的药物,其中很多仅在各种动物模型中验证了效果并且探讨了机制。在这里我们重点讨论的是已经在各种临床慢性肝病中应用过的抗纤维化药物,特别是探讨了近5年来进行的临床试验中这些药物的疗效。
1、皮质类固醇激素:皮质类固醇常被用做各种肝病时的抗炎症药物,但是目前仅在两类慢性肝病时证实有效。一类是自身免疫性肝炎,2004年Czaja等报道87例自身免疫性肝炎患者应用皮质类固醇平均治疗5年的结果,通过对325个肝活组织样本分析提示,53%患者的纤维化积分改善,26%患者纤维化无进展。与以前报道的临床疗效一致。另一类是重症酒精性肝炎特别是对有脑病症状的患者,类固醇短期治疗者存活期延长,但2006年Phillips等报道认为这种对生存率的提高在1年后变得不再显著。
2、秋水仙碱:是一种植物碱类,其机制是通过抑制胶原分泌过程中的微管聚合达到抑制纤维化的目的。从1986年开始报道对原发性胆汁性肝硬化患者的许多生物化学指标有改善,但是没有减轻纤维化。然而1988年Kershenobich等报道了秋水仙碱治疗酒精性肝炎和其他多种肝病纤维化患者的随机双盲临床试验,对100例患者随访了14年,结果表明秋水仙碱不仅可以改善纤维化,还可以显著提高患者生存率。但是此项研究被质疑方法学有问题而没有常规应用于临床。随后进行的多项荟萃分析和2005年Morgan等用秋水仙碱治疗酒精性肝硬化的随机双盲临床试验中,秋水仙碱对于纤维化和生存率均没有明显改善。
3、水飞蓟素:水飞蓟素是植物乳蓟的活性成分,可以有抗脂质过氧化和纤维形成的作用。所有临床研究证实其使用是安全的,但是对抗纤维化的结果不一致。Ferenci等报道在酒精性肝硬化中,水飞蓟素可以降低病死率,早期肝硬化缓解。但Parés等报道200例肝活组织检查或腹腔镜证实有酒精性肝硬化的患者,进行随机双盲安慰剂对照试验,结果却不支持水飞蓟素可以改善酒精性肝硬化患者的生存率。2002年Lucena等其他小样本研究也发现6个月的短期临床治疗仅有抗脂质过氧化等作用。
肝纤维化4.干扰素(干扰素α和干扰素γ):Poynard等报道四个临床试验的3010例初治的丙型肝炎纤维化患者用干扰素α联合利巴韦林治疗24周,以METAVIR积分减轻最少1期为标准,大多患者的纤维化都比治疗前有所减轻。入组时有肝硬化的患者中,49%有肝硬化逆转。纤维化的减轻与开始的纤维化程度、对病毒应答率、病毒水平与年龄和体重均有关。干扰素γ虽然抗病毒的效果弱于干扰素α,但是可以通过抑制星状细胞的细胞外基质合成等机制产生抗肝纤维化效果。Muir等报道对20例干扰素α治疗无效或不能耐受的丙型肝炎患者,用干扰素γ治疗24周,治疗前后做肝穿刺检查。结果提示应用干扰素γ是安全的,有30%的患者有纤维化改善。Weng等用干扰素γ治疗99例乙型肝炎肝纤维化患者,疗程9个月,通过肝活组织检查,治疗组有63%,对照组有21%的患者肝纤维化有改善。
5、熊去氧胆酸:熊去氧胆酸可以通过稳定细胞膜的细胞保护作用减轻炎症和纤维形成。Poupon等对367例原发性胆汁性肝硬化患者用熊去氧胆酸治疗2年,随机对照研究提示可以减轻纤维化,特别是在开始阶段Ⅰ/Ⅱ期的早期的患者,可以显著改善纤维化的进展。除了原发性胆汁性肝硬化以外,熊去氧胆酸可以减轻儿童的家族性肝内胆汁淤积和囊性纤维化的纤维化形成。Lindor等报道166例非酒精性脂肪性肝炎患者的随机、安慰剂对照研究,随访2年的配对肝活组织检查,提示熊去氧胆酸对肝纤维化,甚至对脂肪肝和炎症坏死均没有改善。Dufour等应用熊去氧胆酸和维生素E联合治疗非酒精性脂肪性肝炎患者的研究,结果提示2年的治疗仅可以改善实验室生物化学指标和脂肪肝程度。
6、多不饱和磷脂酰胆碱:对肝脏炎症和纤维形成中的氧化应激过程进行有效的抗氧化作用。Lieber等报道对789例酒精性肝病患者的随机、双盲、安慰剂对照试验中,观察持续2年时间后,由于没有料想到入选患者的平均每日饮酒量从224g乙醇减少至35g乙醇,结果显示多不饱和磷脂酰胆碱没有比安慰剂更显著地改善纤维化,但是对一些亚组患者多不饱和磷脂酰胆碱可以降低转氨酶和胆红素。
7、白细胞介素(IL)-10:IL-10是抗炎和免疫抑制的细胞因子,通过减少炎症前细胞因子肿瘤坏死因子α和IL-1等减轻炎症反应,并使T细胞向Th2转化。Nelson等报道IL-10治疗抗病毒无效的30例丙型肝炎肝纤维化患者的1年试验中,IL-10可以减轻肝内炎症和纤维化,但是HCV-RNA从治疗开始的12.3mEq/ml增加到38mEq/ml。这使得病毒性肝炎患者长期应用IL-10受到了质疑。
8、氯沙坦:肾素-血管紧张素-醛固酮系统在纤维化形成中有重要作用。其主要的效应因子血管紧张素Ⅱ可以通过诱导转化生长因子β1表达刺激胶原沉积。应用血管紧张素转换酶抑制剂氯沙坦可以观察到肝组织纤维化程度减轻。Yokohama等观察了7例非酒精性脂肪性肝炎合并高血压的患者,口服氯沙坦48周后有4例肝组织学纤维化改善,与丙型肝炎肝硬化后肝移植患者的回顾性试验研究结果相似。
9、吡非尼酮(Pirfenidone):2005年Azuma报道包括107例肺间质纤维化患者的随机、双盲、安慰剂对照的临床研究,结果提示患者的氧和能力显著改善,肺功能急性加重频率显著降低,治疗组生存率显著提高。随后在多种肝纤维化动物模型中证实了吡非尼酮可阻断纤维化,表现为病理纤维化评分改善、组织胶原含量降低、α-平滑肌肌动蛋白阳性细胞减少等,同时伴有转化生长因子β1表达下降、促进胶原降解的基质金属蛋白酶表达上调等。2006年Armenda'riz-Borunda等报道应用吡非尼酮(1200mg/d)治疗丙型肝炎肝硬化患者15例的小样本临床研究,疗程12周,治疗前后肝活组织检查比较,53%患者肝脏炎症指数改善,30%Ishak肝纤维化分期降低,60%患者脂肪变性好转。
10、复方牛胎肝提取物:蔡卫民等做了复方牛胎肝提取物片治疗大鼠肝纤维化的实验研究,结果显示:治疗组大鼠死亡数和肝纤维化组织学半定量计分,明显低于对照组。李谦等采用多中心、自身对照研究,观察复方牛胎肝提取物片治疗115例肝纤维化患者的效果,患者口服复方牛胎肝提取物片2片/次,3次/d,治疗24周,治疗前均做肝活组织检查,其中有38例患者在治疗后再次做肝活体组织检查。结果显示:血清肝纤维化标志物透明质酸、层黏连蛋白、Ⅳ型胶原蛋白,治疗后24周和36周,较治疗前(0周)比较显著降低,差异有统计学意义。肝活组织病理检查显示,治疗后肝组织纤维化分期比治疗前有明显降低(P<0.01)。
不良后果
如果治疗不当主要可通过两大危害形成肝硬化:一是由于肝组织结构的破坏,使肝内血管受压扭曲、闭锁或动脉与静脉之间出现“短路”吻合,造成门静脉系统血管阻力增大,形成门静脉高压,导致脾肿大、腹水生成和胃底食管静脉曲张,有上消化道曲张静脉破裂出血的潜在危险;二是正常肝细胞之间的血液微循环通道因纤维组织成分的沉积而造成循环障碍,影响肝细胞的血液供应,使因炎症受损的肝细胞不易修复甚至加重损伤,直至功能正常的肝细胞愈来愈少,最后导致肝功能衰竭。两大危害都是致命的。
预防保健
1.情绪稳定:肝脏与精神情志的关系非常密切。情绪不佳,精神抑郁,暴怒激动均可影响肝的机能,加速病变的发展。树立坚强意志,心情开朗,振作精神,消除思想负担,会有益于病情改善。
2.动静结合:肝纤维化代偿功能减退,并发腹水或感染时应绝对卧床休息。在代偿功能充沛、病情稳定期可做些轻松工作或适当活动,进行有益的体育锻炼,如散步、做保健操、太极拳、气功等。活动量以不感觉到疲劳为度。
3.用药从简:盲目过多地滥用一般性药物,会加重肝脏负担,不利于肝脏恢复。对肝脏有害的药物如异烟肼、巴比妥类应慎用或忌用。
4.戒烟忌酒:酒能助火动血,长期饮酒,尤其是烈性酒,可导致酒精性肝硬化。因此,饮酒可使肝硬化患者病情加重,并容易引起出血。长期吸烟不利于肝病的稳定和恢复,可加快肝硬化的进程,有促发肝癌的危险。
5.饮食调护:以低脂肪、高蛋白、高维生素和易于消化饮食为宜。做到定时、定量、有节制。早期可多吃豆制品、水果、新鲜蔬菜,适当进食糖类、鸡蛋、鱼类、瘦肉;当肝功能显著减退并有肝昏迷先兆时,应对蛋白质摄入适当控制,提倡低盐饮食或忌盐饮食。食盐每日入量不超过1~1.5克,饮水量在2000毫升内,严重腹水时,食盐摄入量应控制在500毫克以内,水摄入量在1000毫升以内。应忌辛辣刺激之品和坚硬生冷食物,不宜进食过热食物以防并发出血。
6.积极预防:肝硬化是由不同原因引起的肝脏实质性变性而逐渐发展的一个后果。
要重视对各种原发病的防治,积极预防和治疗慢性肝炎、血吸虫病、胃肠道感染,避免接触和应用对肝脏有毒的物质,减少致病因素。
肝纤四项
肝纤四项即肝纤维化四项检查,该检查主要用来检查诊断慢性肝病患者病情发展状况和治疗效果,衡量炎症活动度、纤维化程度的重要依据。诊断肝纤维化需要进行肝纤四项检查。肝纤四项主要包括以下四个检查指标:
1. PCIII (III型前胶原):反映肝内III型胶原合成,血清含量与肝纤程度一致,并与血清γ-球蛋白水平明显相关。PCIII与肝纤维化形成的活动程度密切相关,但无特异性,其它器官纤维化时,PCIII也升高。持续PCIII升高的慢活肝,提示病情可能会恶化并向肝硬变形成发展,而PCIII降至正常可预示病情缓解,说明PCIII 不仅在肝纤维化早期诊断上有价值,在慢性肝病的预后判断上也有意义。
血清PCⅢ水平与肝纤维化病变程度呈密切相关,反映肝纤维合成状况和炎症活动性,早期即显著升高,而陈旧性肝硬化和部分晚期肝硬变、肝萎缩患者血清PCⅢ不一定增高。
2. IV-C(IV型胶原):为构成基底膜主要成份,反映基底膜胶原更新率,含量增高可较灵敏反映出肝纤过程,是肝纤的早期标志之一。
(1) 在肝纤维化时出现最早,适合于肝纤维化的早期诊断。
(2) 能反映肝纤维化程度,随着慢迁肝→慢活肝→肝硬化→肝癌病程演病,Ⅳ-C胶原在血清含量逐步升高。
(3)对重症肝炎和酒精性肝炎也显高值。
(4)是药物疗效和预后观察重要依据,血清Ⅳ-C水平与肝组织学的改变完全一致。
(5)在与基底膜相关疾病可出现Ⅳ-C水平的异常,如甲状腺机能亢进,中晚期糖尿病、硬皮病等。
3. LN(层粘连蛋白):为基底膜中特有的非胶原性结构蛋白,与肝纤维化活动程度及门静脉压力呈正相关,慢活肝和肝硬变及原发性肝癌时明显增高 ,LN也可以反映肝纤维化的进展与严重程度。另外,LN水平越高,肝硬变病人的食管静脉曲张越明显。
(1) 反映肝纤维化:正常肝脏间质含少量LN,在肝纤维化和肝硬化时, →肌成纤维细胞增多→大量合成和分泌胶原、LN等间质成分→形成完整的基底膜(肝窦毛细血管化)。肝窦毛细血管化是肝硬化的特征性病理改变, LN与纤维化程度和门脉高压正相关,纤维化后期升高尤为显著。
(2) 与肿瘤浸润、转移有关:癌症转移首先要突破基底膜,因此LN与肿瘤浸润转移有关。大部分肿瘤患者血清LN水平升高,尤以乳腺癌、肺癌、结肠癌、胃癌显著。
(3) 与基底膜相关疾病有关:如先兆子痫孕妇血清较正常妊娠者显著升高,提示可能与肾小球及胎盘螺旋动脉损伤有关。血清LN与糖尿病、肾小球硬化等疾病有关。
4. HA(透明质酸酶):为基质成分之一,由间质细胞合成,可较准确灵敏地反映肝内已生成的纤维量及肝细胞受损状况,有认为本指标较之肝活检更能完整反映出病肝全貌,是肝纤维化和肝硬变的敏感指标。
(1) 血清HA在急肝、慢迁肝时轻度升高;慢活肝时显著升高;肝硬化时极度升高。
(2) 肝硬化病人血清HA极度升高。
(3) HA水平与血清胆红素、SGPT(Serum glutamic-pyruvic 血清谷丙转氨酶)、γ-球蛋白呈正相关
(5) 故血清HA水平是反映肝损害严重程度、判断有无活动性肝纤维化的定量指标 。
(6) 对慢迁肝与慢活肝的鉴别诊断,慢迁肝HA浓度与正常人无差别,而慢活肝的升高明显。
(7) 有助于估价肝病发展趋势,在急性肝炎→慢活肝→肝硬化发展中,血清HA逐步并优于其他肝硬化诊断指标等。